Wesentliche elektronische Materialien: Teil 5 - Materialien auf Kohlenstoffbasis
1 Einleitung
Materialien auf Kohlenstoffbasis haben sich aufgrund ihrer außergewöhnlichen physikalischen, chemischen und elektronischen Eigenschaften als transformative Elemente in elektronischen Materialien erwiesen. Graphen, Kohlenstoff-Nanoröhren (CNTs) und Fullerene zeichnen sich als vielseitige Materialien aus, deren Anwendungen von Hochgeschwindigkeitstransistoren bis hin zu fortschrittlichen Energiespeichern reichen. Die bemerkenswerte Leitfähigkeit und mechanische Festigkeit von Graphen, die einzigartige eindimensionale Struktur und Flexibilität von CNTs und die ausgeprägte Molekülkonfiguration und die Halbleitereigenschaften von Fullerenen haben sie gemeinsam zu zentralen Komponenten in der modernen Elektronik gemacht. Dieser Artikel befasst sich mit diesen Materialien und geht auf ihre Prinzipien, Vorteile und realen Anwendungen in elektronischen Geräten ein. Er zeigt, wie Kohlenstoff die Möglichkeiten in Elektronik und Technologie neu definiert.
2 Graphen
Graphen ist ein Allotrop des Kohlenstoffs, bei dem die Kohlenstoffatome in sp²-Hybridisierung zu einer einzigen hexagonalen Wabengitter-Graphenschicht verbunden sind. Fullerene (C60), Graphen-Quantenpunkte, Kohlenstoff-Nanoröhren, Nanobänder, mehrwandige Kohlenstoff-Nanoröhren und Nanohörner können mit dieser kristallinen Struktur von Graphen hergestellt werden. Gestapelte Graphenschichten (mehr als 10 Schichten) bilden Graphit, wobei die Schichten durch van-der-Waals-Kräfte zusammengehalten werden und der Abstand zwischen den Kristallebenen 0,335 Nanometer beträgt. Graphen hat hervorragende optische, elektrische und mechanische Eigenschaften und findet wichtige Anwendungen in der Materialwissenschaft, der Mikro- und Nanofabrikation, der Energietechnik, der Biomedizin und der Medikamentenverabreichung und gilt als revolutionäres Material der Zukunft.
2.1 Struktur und Eigenschaften von Graphen
Die Anordnung der Kohlenstoffatome im Inneren von Graphen ist mit sp2-hybridisierten Orbitalen wie in monatomaren Graphitschichten gebunden und weist folgende Merkmale auf: Kohlenstoffatome haben vier Valenzelektronen, von denen drei sp2-Bindungen erzeugen, d. h., jedes Kohlenstoffatom steuert ein nicht gebundenes Elektron bei, das sich in den pz-Orbitalen befindet, die pz-Orbitale der nahen Nachbaratome sind senkrecht zur Ebene ausgerichtet und können zu einer π-Bindung geformt werden, die neu gebildeten π-Bindungen sind im halbgefüllten Zustand. Die Studie bestätigt, dass die Koordinationszahl der Kohlenstoffatome in Graphen 3 ist, die Bindungslänge zwischen jeweils zwei benachbarten Kohlenstoffatomen 1,42 × 10-10 m beträgt und der Winkel zwischen der Bindung und der Bindung 120° ist. Zusätzlich zu den σ-Bindungen, die sich mit anderen Kohlenstoffatomen zu einer wabenförmigen Schichtstruktur eines hexagonalen Rings verbinden, können die pz-Orbitale, die senkrecht zur Schichtebene jedes Kohlenstoffatoms stehen, große π-Bindungen mit mehreren Atomen bilden, die sich durch die gesamte Schicht ziehen (ähnlich wie Benzolringe), was zu einer hervorragenden elektrischen Leitfähigkeit und optischen Eigenschaften führt.

Abb. 1 Graphen ist eine einlagige Struktur aus Kohlenstoffatomen
Graphen hat bei Raumtemperatur eine Ladungsträgerbeweglichkeit von etwa 15.000 cm2/(V-s), ein Wert, der mehr als zehnmal so hoch ist wie der von Silizium und mehr als doppelt so hoch wie der von Indiumantimonid (InSb), dem Stoff mit der höchsten bekannten Ladungsträgerbeweglichkeit. Unter bestimmten Bedingungen, z. B. bei niedrigen Temperaturen, kann die Ladungsträgerbeweglichkeit von Graphen sogar 250.000 cm2/(V-s) betragen. Im Gegensatz zu vielen anderen Materialien wird die Elektronenbeweglichkeit von Graphen durch Temperaturänderungen weniger beeinträchtigt, und die Elektronenbeweglichkeit von einlagigem Graphen liegt bei einer Temperatur zwischen 50 und 500 K bei etwa 15.000 cm2/(V-s).
Darüber hinaus kann der halbzahlige Quanten-Hall-Effekt von Elektronen- und Lochträgern in Graphen beobachtet werden, indem das chemische Potenzial durch die Einwirkung eines elektrischen Feldes verändert wird, und Wissenschaftler haben diesen Quanten-Hall-Effekt in Graphen bei Raumtemperatur beobachtet. Die Ladungsträger in Graphen folgen einem speziellen Quantentunneleffekt und streuen nicht zurück, wenn sie auf Verunreinigungen treffen, was der Grund für die lokale Supraleitfähigkeit von Graphen und seine sehr hohe Ladungsträgerbeweglichkeit ist. Weder Elektronen noch Photonen haben in Graphen eine Ruhemasse; ihre Geschwindigkeit ist eine Konstante, die nichts mit der kinetischen Energie zu tun hat.
Graphen ist ein Halbleiter mit Nullbereich, da sich seine Leitungs- und Valenzbänder am Dirac-Punkt treffen. Die Brillouin-Zone, der Rand des Impulsraums an den sechs Positionen des Dirac-Punkts, ist in zwei Gruppen von gleichwertigen Tripletts unterteilt. Im Gegensatz dazu haben herkömmliche Halbleiter typischerweise Γ als Hauptpunkt mit Nullimpuls.
2.2 Anwendungen von Graphen
Integrierte Schaltungen: Graphen hat aufgrund seiner hervorragenden elektrischen und thermischen Leitfähigkeit ein großes Potenzial im Bereich der integrierten Schaltungen. So hat IBM erfolgreich integrierte Schaltkreise aus Graphen-Wafern entwickelt, die als Breitband-HF-Mixer bis zu 10 GHz arbeiten. Darüber hinaus wurde Graphen bei der Herstellung von integrierten 3D-Schaltungen eingesetzt, um Probleme mit der Wärmeableitung und elektromagnetischen Störungen zu lösen.
Feldeffekttransistoren (FETs): Graphen-FETs eignen sich aufgrund ihrer hohen Ladungsträgerbeweglichkeit und atomaren Dicke ideal als Kanalmaterialien. Graphen-FETs werden sowohl in analogen als auch in digitalen Schaltungen eingesetzt. In analogen Schaltungen können Graphen-FETs für HF-Anwendungen verwendet werden; in digitalen Schaltungen können Methoden wie chemische Dotierung die Bandlücke von Graphen öffnen und sein Schaltstromverhältnis verbessern, wodurch sein Potenzial für den Einsatz in digitalen Logikbausteinen erhöht wird.
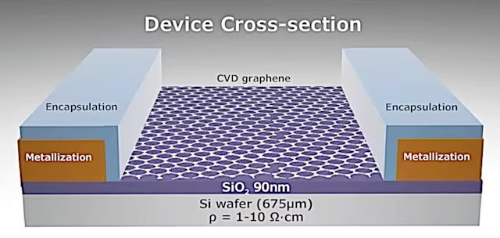
Abb. 2 Aufbau eines Graphen-Feldeffekttransistors (GFET)
Organische lichtemittierende Diode (OLED): Graphen wird als transparente leitende Elektrode für OLEDs verwendet und ersetzt aufgrund seiner Lichtdurchlässigkeit und Leitfähigkeit das traditionelle ITO-Material. OLED-Bauelemente mit Graphenelektroden sind hinsichtlich ihrer optischen und mechanischen Eigenschaften mit ITO-Elektroden vergleichbar, und Graphen ist flexibler, was die Herstellung von biegsamen Anzeigegeräten begünstigt.
Chemische Sensoren: Die hohe spezifische Oberfläche von Graphen und seine Empfindlichkeit gegenüber der Umwelt verleihen ihm ein großes Potenzial auf dem Gebiet der chemischen Sensoren. Chemische Sensoren aus Graphen können zum Nachweis verschiedener Gase wie NO2 und NH3 mit hoher Empfindlichkeit und niedrigen Nachweisgrenzen verwendet werden.
Optoelektronische Geräte: Graphen hat aufgrund seiner einzigartigen physikalisch-chemischen Eigenschaften ein großes Potenzial im Bereich der optoelektronischen Geräte. Zu seinen Vorteilen gehören hohe elektrische Leitfähigkeit, breite spektrale Absorption, ultraschnelle Ladungsträgerbeweglichkeit und gute mechanische Flexibilität. Die breiten spektralen Absorptionseigenschaften und die schnelle elektronische Dynamik von Graphen ermöglichen eine effiziente Detektion vom Ultraviolett bis zum fernen Infrarot in Photodetektoren und eignen sich für Hochgeschwindigkeits-Glasfaserkommunikation und Terahertz-Detektion. Als transparentes, leitfähiges Material wird Graphen häufig in organischen Solarzellen und Chalkogenid-Solarzellen verwendet, um die photovoltaische Umwandlungseffizienz zu verbessern und flexible, tragbare Geräte zu unterstützen. Es kann auch als transparente Anode in Leuchtdioden verwendet oder mit anderen Materialien kombiniert werden, um die Lumineszenzeigenschaften für flexible Displays und OLED-Geräte zu verbessern. Darüber hinaus wird Graphen aufgrund seiner hohen nichtlinearen optischen Reaktion häufig in optischen Modulatoren und ultraschnellen Lasern eingesetzt, die eine effiziente Modulation optischer Signale und die Ausgabe ultrakurzer Laserimpulse ermöglichen. Seine Flexibilität und Transparenz unterstützen auch die Entwicklung flexibler optoelektronischer Geräte wie gekrümmte Displays und elektronische Häute.
3 Kohlenstoff-Nanoröhrchen (CNTs)
Kohlenstoff-Nanoröhren, ein eindimensionales Quantenmaterial mit einer besonderen Struktur, haben radiale Abmessungen in der Größenordnung von Nanometern und axiale Abmessungen in der Größenordnung von Mikrometern, und die Röhre ist im Wesentlichen an beiden Enden versiegelt. Kohlenstoff-Nanoröhren bestehen hauptsächlich aus Kohlenstoffatomen, die in einem hexagonalen Muster angeordnet sind und koaxiale, kreisförmige Röhren mit mehreren bis Dutzenden von Schichten bilden. Der Abstand zwischen den Schichten ist auf etwa 0,34 nm festgelegt, und der Durchmesser beträgt im Allgemeinen 2-20 nm. Die Kohlenstoff-Nanoröhren können entsprechend der unterschiedlichen Ausrichtung der Kohlenstoffsechsecke in axialer Richtung in Sägezahn-, Sessel- und Spiralröhren eingeteilt werden. Die spiralförmigen Kohlenstoff-Nanoröhren weisen Chiralität auf, während die sägezahn- und armchairartigen Kohlenstoff-Nanoröhren keine Chiralität aufweisen.
3.1 Struktur und Eigenschaften von Kohlenstoff-Nanoröhren
Die Kohlenstoffatome in Kohlenstoff-Nanoröhren sind überwiegend sp2-hybridisiert, während die hexagonale Gitterstruktur einen gewissen Grad an Biegung aufweist und eine räumliche Topologie bildet, die bestimmte sp3-hybridisierte Bindungen bilden kann, d. h. die Bildung chemischer Bindungen zur gleichen Zeit mit einer gemischten Hybridisierung des sp2- und sp3-Zustands, und diese p-Orbitale überlappen einander, um hoch exotisierte große π-Bindungen außerhalb der Kohlenstoff-Nanoröhren-Graphenschicht zu bilden. Die großen π-Bindungen an der Außenfläche der Kohlenstoff-Nanoröhren sind die chemische Grundlage für die nicht-kovalente Bindung zwischen Kohlenstoff-Nanoröhren und einigen Makromolekülen mit Konjugationseigenschaften.
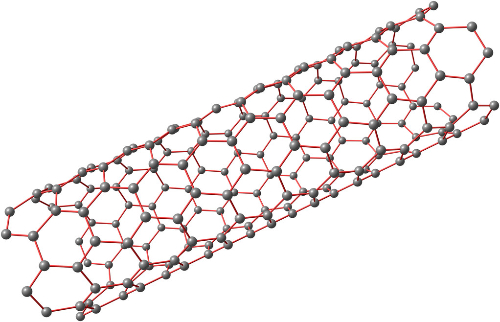
Abb. 3 Struktur von Kohlenstoff-Nanoröhren
Die Ergebnisse der Photoelektronenspektroskopie von mehrwandigen Kohlenstoffnanoröhren zeigen, dass sowohl einwandige als auch mehrwandige Kohlenstoffnanoröhren bestimmte funktionelle Gruppen auf ihrer Oberfläche vereinen, und dass die durch verschiedene Präparationsmethoden gewonnenen Kohlenstoffnanoröhren aufgrund der unterschiedlichen Präparationsmethoden und Nachbearbeitungsprozesse unterschiedliche Oberflächenstrukturen aufweisen. Im Allgemeinen haben einwandige Kohlenstoff-Nanoröhren eine höhere chemische Inertheit und ihre Oberflächen sind reiner, während die Oberflächen von mehrwandigen Kohlenstoff-Nanoröhren viel aktiver sind und eine große Anzahl von Oberflächengruppen, wie z. B. Carboxylgruppen, enthalten. Die Ergebnisse des Oberflächennachweises von Kohlenstoff-Nanoröhren durch Röntgen-Elektronenspektroskopie mit variablem Winkel zeigen, dass die Oberfläche von einwandigen Kohlenstoff-Nanoröhren chemisch inert und die chemische Struktur relativ einfach ist, während mit zunehmender Anzahl der Schichten der Kohlenstoff-Nanoröhrenwand die Defekte und die chemische Reaktivität zunehmen und die chemische Struktur der Oberfläche eher kompliziert ist. Die chemische Struktur der inneren Schicht aus Kohlenstoffatomen ist relativ einfach, die chemische Zusammensetzung der äußeren Schicht aus Kohlenstoffatomen ist komplexer, und auf der äußeren Schicht aus Kohlenstoffatomen ist oft eine große Menge amorpher Kohlenstoff abgelagert. Aufgrund der Inhomogenität der physikalischen und chemischen Strukturen haben viele Oberflächenkohlenstoffatome in Kohlenstoffnanoröhren unterschiedliche Oberflächenmikroumgebungen und weisen daher auch energetische Inhomogenität auf.
Kohlenstoff-Nanoröhren sind nicht immer gerade, sondern weisen örtlich begrenzte konvexe und konkave Bereiche auf, die auf die Entstehung von Fünfecken und Siebenecken bei der hexagonalen Präparation zurückzuführen sind. Wenn das Fünfeck genau an der Spitze des Kohlenstoff-Nanoröhrchens erscheint, bildet es die Dichtung des Kohlenstoff-Nanoröhrchens. Wenn das Heptagon erscheint, ist das Nanoröhrchen konkav. Diese topologischen Defekte können die spiralförmige Struktur von Kohlenstoffnanoröhren verändern, und auch die elektronische Energiebandstruktur in der Nähe der Defekte wird verändert. Außerdem sind zwei benachbarte Kohlenstoffnanoröhren nicht direkt miteinander verklebt, sondern werden auf Abstand gehalten.
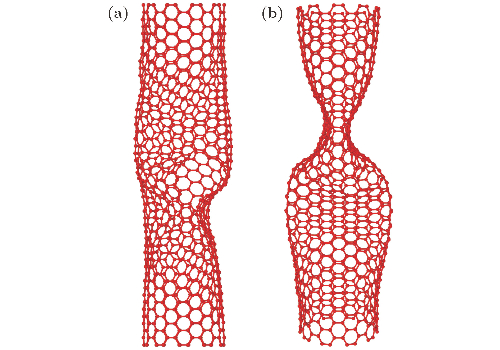
Abb. 4 Knickinstabilitätskonfiguration von Kohlenstoffnanoröhren mit polyatomaren Vakanzdefekten unter axialer Belastung: (a) Kohlenstoffnanoröhren mit polyatomaren Vakanzdefekten, die entlang der axialen Richtung verteilt sind; (b) Kohlenstoffnanoröhren mit polyatomaren Vakanzdefekten, die entlang der Umfangsrichtung verteilt sind.[1]
Die P-Elektronen der Kohlenstoffatome in Kohlenstoff-Nanoröhren bilden eine Vielzahl von π-Bindungen außerhalb der Domäne, und aufgrund des bedeutenden Konjugationseffekts haben Kohlenstoff-Nanoröhren einige besondere elektrische Eigenschaften. Bei metallischen Kohlenstoffnanoröhren überlappen sich das Valenzband und das Leitungsband teilweise, was einem halbvollen Energieband entspricht. Die Elektronen können sich frei bewegen und zeigen eine metallähnliche Leitfähigkeit, während halbleitende Kohlenstoffnanoröhren eine kleine Bandlücke zwischen dem Valenzband und dem Leitungsband aufweisen und die Valenzbandelektronen bei Raumtemperatur in das Leitungsband springen können, um Strom zu leiten.
Kohlenstoff-Nanoröhren haben eine gute elektrische Leitfähigkeit, da die Struktur von Kohlenstoff-Nanoröhren mit der lamellaren Struktur von Graphit identisch ist. Die Theorie sagt voraus, dass ihre elektrische Leitfähigkeit von ihrem Rohrdurchmesser und dem Schrägungswinkel der Rohrwand abhängt. Wenn der Röhrendurchmesser von CNTs größer als 6 nm ist, nimmt die elektrische Leitfähigkeit ab; wenn der Röhrendurchmesser kleiner als 6 nm ist, können CNTs als eindimensionale Quantendrähte mit guter elektrischer Leitfähigkeit angesehen werden. Es wurde berichtet, dass Huang Kohlenstoffnanoröhren mit einem Durchmesser von 0,7 nm durch Berechnungen als supraleitend eingestuft hat, und obwohl ihre supraleitende Übergangstemperatur nur 1,5 × 10-4 K beträgt, ist dies ein Vorbote der Aussichten von Kohlenstoffnanoröhren auf dem Gebiet der Supraleitung.
Der Vektor Ch wird üblicherweise verwendet, um die Richtung der atomaren Anordnung auf Kohlenstoff-Nanoröhren darzustellen, wobei Ch = na1 + ma2, bezeichnet als (n, m). wobei a1 und a2 jeweils die beiden Basisvektoren bezeichnen und (n, m) eng mit der elektrischen Leitfähigkeit von Kohlenstoff-Nanoröhren zusammenhängt. Wenn für ein gegebenes (n, m)-Nanoröhrchen 2n + m = 3q gilt (q ist eine ganze Zahl), dann weist diese Richtung Metallizität auf und ist ein guter Leiter, ansonsten verhält sie sich wie ein Halbleiter. In der Richtung n = m weisen Kohlenstoffnanoröhren eine gute elektrische Leitfähigkeit auf, die typischerweise bis zum 10.000-fachen der Leitfähigkeit von Kupfer reicht.
3.2 Anwendungen von Kohlenstoff-Nanoröhrchen
EFETs: Kohlenstoffnanoröhren haben eine ausgezeichnete elektronische Leitfähigkeit und thermische Stabilität, was sie ideal für die Herstellung von Hochleistungs-EFETs macht. E-Feld-Bauelemente wie Bildröhren, Leuchtstoffschirme und Mikrolaser werden hauptsächlich in der Mikro- und Optoelektronik eingesetzt. Diese Eigenschaften von Kohlenstoffnanoröhren verbessern die Emissionsleistung dieser Geräte erheblich.
Elektronische Sensoren: Kohlenstoff-Nanoröhren werden auch häufig in elektronischen Sensoren eingesetzt. Aufgrund ihrer extrem hohen Empfindlichkeit können sie kleine physikalische Veränderungen in ihrer Umgebung wahrnehmen und bleiben auch unter extremen Bedingungen wie hohen Temperaturen stabil. Kohlenstoff-Nanoröhren gewinnen als neues Sensormaterial an Aufmerksamkeit, insbesondere im Bereich der flexiblen Elektronik.
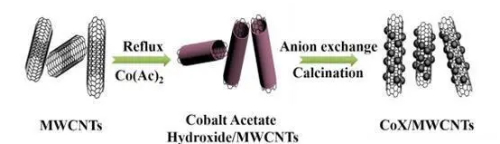
Abb. 5 Kobalt-Manganoxid-Kohlenstoffnanoröhren-Verbundwerkstoffe für eine verbesserte Leistung in Sensoren
Solarzellen: Kohlenstoff-Nanoröhrchen wurden auch in Solarzellen mit bemerkenswerten Ergebnissen eingesetzt. Obwohl die spezifischen Details in den Suchergebnissen nicht detailliert beschrieben sind, kann spekuliert werden, dass ihre Anwendung bei photovoltaischen Effekten die Effizienz und Stabilität von Solarzellen verbessern könnte.
4 Fullerene
Fulleren, ein Hohlmolekül, das vollständig aus Kohlenstoff besteht, ist kugelförmig, ellipsoidisch, säulenförmig oder röhrenförmig. Fulleren ähnelt strukturell dem Graphit, der aus Schichten von Graphen besteht, die mit sechsgliedrigen Ringen gestapelt sind, während Fulleren nicht nur sechsgliedrige Ringe, sondern auch fünfgliedrige Ringe und gelegentlich siebengliedrige Ringe enthält. Je nach der Gesamtzahl der Kohlenstoffatome können Fullerene in die Kategorien C20, C60, C70, C76, C80 usw. eingeteilt werden. Das kleinste Fulleren unter ihnen ist C20. Die hochsymmetrische, käfigartige Struktur von C60 verleiht ihm eine hohe Stabilität und ist daher das am meisten untersuchte Fulleren.
Abb. 6 Struktur der Fullerene
Fullerene sind aufgrund ihrer einzigartigen nulldimensionalen Struktur eines der wichtigsten kohlenstoffhaltigen Nanomaterialien der letzten Jahre. Fullerene haben besondere optische Eigenschaften, elektrische Leitfähigkeit und chemische Eigenschaften, so dass Fullerene und ihre Derivate in der Elektrizitäts-, Licht-, Magnetismus- und Materialwissenschaft breite Anwendung finden.
4.1 Struktur und Eigenschaften von Fullerenen
Mathematisch gesehen sind alle Fullerene als konvexe Polyeder mit fünfeckigen und sechseckigen Flächen aufgebaut. Das kleinste Fulleren ist C20 mit einer ortho-dodekaedrischen Konfiguration. Es gibt keine Fullerene mit 22 Eckpunkten, danach folgen alle Fullerene mit C2n, n=12, 13, 14 usw. Die Anzahl der Fünfecke in allen Fulleren-Strukturen ist 12 und die Anzahl der Sechsecke ist n-10.
Nachdem es möglich war, C60 in großen Mengen herzustellen, wurden viele seiner Eigenschaften entdeckt. Haddon et al. fanden bald heraus, dass sich mit Alkalimetallen dotiertes C60 metallisch verhält, und 1991 wurde festgestellt, dass mit Kalium dotiertes C60 bei 18 K supraleitend ist - dies ist die bisher höchste molekulare Supraleitungstemperatur. Es wurde gezeigt, dass die supraleitende Übergangstemperatur mit dem Zellvolumen von Alkalimetall-dotierten Fullerenen zunimmt. Da Cäsium die größten Alkalimetallionen bilden kann, wurden cäsiumdotierte Fullerenmaterialien eingehend untersucht, und kürzlich wurde über die supraleitenden Eigenschaften von Cs3C60As bei 38 K berichtet, allerdings bei hohem Druck. Das Material mit der höchsten supraleitenden Übergangstemperatur bei 33 K und Atmosphärendruck ist Cs2RbC60. Die BCS-Theorie der Supraleitung in C60-Festkörpern legt nahe, dass die supraleitende Übergangstemperatur mit zunehmendem Zellvolumen ansteigt, weil der Abstand zwischen den C60-Molekülen mit einer Zunahme der Zustandsdichte auf dem Fermi-Energieniveau N (εF) korreliert. Daher haben Wissenschaftler viel unternommen, um die Abstände zwischen den Fulleren-Molekülen zu vergrößern, insbesondere durch Einfügen neutraler Moleküle in das A3C60-Gitter, um den Abstand zu vergrößern, während die Valenz von C60 unverändert bleibt. Diese Aminierungstechnik führte jedoch unerwartet zu neuen und besonderen Eigenschaften der Fulleren-Insertionskomplexe: dem Mott-Hubbard-Übergang und der Beziehung zwischen der Orientierung/Orbitalordnung der C60-Moleküle und der magnetischen Struktur. Der C60-Festkörper besteht aus schwach wechselwirkenden Kräften und ist daher ein molekularer Festkörper, der die Eigenschaften eines Moleküls beibehält. Die diskreten Energieniveaus eines freien C60-Moleküls sind im Festkörper nur schwach diffundiert, was zu einer schmalen, nicht überlappenden Bandlücke im Festkörper von nur 0,5 eV führt. Bei undotierten C60-Festkörpern mit einem 5-fachen hu-Band als HOMO-Energieniveau und einem 3-fachen t1u-Band als leerem LUMO-Energieniveau ist dieses System bandverboten. Wenn der C60-Festkörper jedoch mit Metallatomen dotiert ist, geben die Metallatome die Elektronen des t1u-Bandes oder einige der Elektronen des dreifachen t1g-Bandes ab, um es zu besetzen, und nehmen manchmal einen metallischen Charakter an. Obwohl das t1u-Band von A4C60 teilweise besetzt ist, sollte es nach der BCS-Theorie metallische Eigenschaften haben, ist aber ein Isolator. Dieses Paradoxon lässt sich durch den Jahn-Teller-Effekt erklären, bei dem die spontane Verformung eines Moleküls mit hoher Symmetrie zur Aufspaltung seiner verketteten Orbitale führt, wodurch es elektronische Energie gewinnt. Diese Jahn-Teller-Wechselwirkung zwischen Elektronen und Phononen ist in C60-Festkörpern so stark, dass sie das Valenzbandmuster eines bestimmten Valenzzustands stören kann. Schmalbandlücken oder starke Elektronenwechselwirkungen und ein kondensierter Grundzustand sind wichtig, um die Supraleitfähigkeit von Fulleren-Festkörpern zu verstehen und zu erklären. Das einfache Mott-Hubbard-Modell erzeugt isolierende, lokalisierte elektronische Grundzustände, wenn die elektronische gegenseitige Abstoßung größer ist als die Bandbreite, was das Fehlen von Supraleitung in cäsiumdotierten C60-Festkörpern bei Atmosphärendruck erklärt. Die Lokalisierung von t1u-Elektronen, die durch elektronische Wechselwirkungen jenseits eines kritischen Punktes angetrieben wird, erzeugt Mott-Isolatoren, und der Einsatz von hohem Druck verringert den Abstand der Fullerene voneinander, woraufhin der cäsiumdotierte C60-Festkörper Metallizität und Supraleitung aufweist.
Es gibt keine vollständige Theorie zur Supraleitung von C60-Festkörpern, aber die BCS-Theorie ist weithin anerkannt, weil starke Elektronenwechselwirkungen und Jahn-Teller-Elektronen-Phonon-Kopplungen Elektronenpaare erzeugen können, die hohe Isolator-Metall-Übergangstemperaturen ergeben.
4.2 Anwendungen von Fullerenen
Kondensatoren: Fullerene haben aufgrund ihrer guten elektrischen Leitfähigkeit und chemischen Stabilität wichtige Anwendungen bei der Herstellung von Hochleistungskondensatoren. Ihre einzigartige Molekularstruktur verbessert die Leitfähigkeit und die Energiespeicherdichte der Elektroden erheblich und erhöht gleichzeitig die Lebensdauer und Zuverlässigkeit der Kondensatoren. Mit Fulleren verstärkte Superkondensatoren sind in der Lage, große Strommengen in kurzer Zeit mit stabiler und effizienter Leistung zu speichern und freizugeben. Sie finden breite Anwendung in elektronischen Geräten und Energiemanagementsystemen und stellen eine hochwertige Lösung für moderne Energiespeicher dar.
Leitfähiger Klebstoff: Fullerene können zur Herstellung leitfähiger Klebstoffe mit ausgezeichneter Leistung verwendet werden, die eine wichtige Rolle bei der Befestigung und Verbindung elektronischer Komponenten spielen. Sie bieten effiziente Elektronentransportwege und verbessern die Leitfähigkeit erheblich. Im Vergleich zu herkömmlichen leitfähigen Klebstoffen haben Fulleren-Leitklebstoffe eine höhere Viskosität und Fließfähigkeit bei gleichzeitig hervorragender Haftung. Sie eignen sich für die Montage elektronischer Präzisionsgeräte wie Chip-Packages, flexible Schaltkreisverbindungen usw. und erfüllen die Nachfrage nach hochzuverlässigen leitfähigen Klebstoffanwendungen.
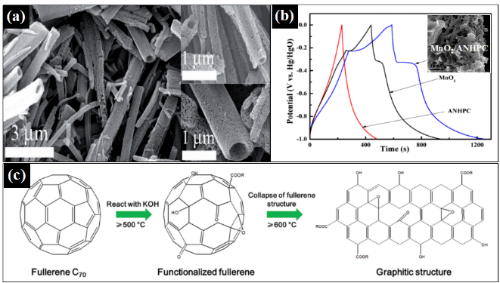
Abb. 7 Anwendung von FMNSs in Superkondensatoren. (a) REM-Aufnahme von C60-μm-Röhren, die durch Hochtemperaturverkohlung hergestellt wurden; (b) Ladungs-Entladungskurven von Fulleren/MnO2-Verbundwerkstoffen (die Einblendung zeigt die REM-Aufnahme der Verbundwerkstoffe); (c) Ladungs-Entladungskurven von C70-μm-Röhren, die durch KOH-Aktivierung hergestellt wurden (die Einblendung zeigt die REM-Aufnahme des porösen Materials).
Optoelektronische Anwendungen: Fulleren, ein Schlüsselmaterial für optoelektronische Geräte, weist hervorragende Elektronenakzeptoreigenschaften und eine n-Typ-Halbleiterleistung auf. Seine geringe Ladungsträgerkomplexwahrscheinlichkeit und hohe Elektronenbeweglichkeit machen es zu einem idealen Material für den Elektronentransport. Fullerenmoleküle (z. B. C60 oder C70) können mit organischen Halbleitermaterialien vom p-Typ gekoppelt werden, um die Effizienz der Ladungstrennung und die Leistungsstabilität der Bauelemente zu verbessern, die in der organischen Photovoltaik (OPV), in organischen Feldeffekttransistoren (OFETs) und in Photodetektoren weit verbreitet sind. In OPVs fungieren Fullerene als Elektronenakzeptoren, um die fotoelektrische Umwandlungseffizienz zu verbessern; in OFETs zeigen ihre Transistoren eine ausgezeichnete Leistung in inerten Umgebungen und eignen sich für Display-Treiber und Fotodetektoren; außerdem verbessern Fullerene die Elektroneninjektion und die Stromübertragungsfähigkeiten von Leuchtdioden (OLEDs) und bieten technische Unterstützung für die Entwicklung hocheffizienter optoelektronischer Geräte.
5 Schlussfolgerung
Die Erforschung von Graphen, Kohlenstoff-Nanoröhren und Fullerenen unterstreicht das enorme Potenzial von Materialien auf Kohlenstoffbasis für die Gestaltung der Zukunft der Elektronik. Ihre einzigartigen Eigenschaften - sei es die unvergleichliche Leitfähigkeit von Graphen, die außergewöhnliche Flexibilität und Zugfestigkeit von CNTs oder das ausgeprägte elektronische und photonische Verhalten von Fullerenen - haben Durchbrüche in verschiedenen Anwendungen wie Transistoren, Sensoren, Kondensatoren und lichtemittierenden Bauteilen ermöglicht. Da die Forschungs- und Fertigungstechnologien weiter voranschreiten, versprechen diese Materialien, bestehende Herausforderungen zu überwinden und den Weg für eine neue Ära innovativer, effizienter und nachhaltiger elektronischer Systeme zu ebnen. Ihre Integration in Spitzentechnologien wird zweifellos den Fortschritt in Bereichen von erneuerbaren Energien bis hin zu Computern der nächsten Generation vorantreiben und die wesentliche Rolle von Kohlenstoff in der Entwicklung der modernen Elektronik festigen.
Stanford Advanced Materials (SAM) ist ein wichtiger Anbieter von hochwertigen kohlenstoffbasierten Materialien und unterstützt diese kritischen Anwendungen mit zuverlässigen Materiallösungen.
Referenz
[1] Wang Lei, Zhang Ran-Ran, Fang Wei. Simulation der statischen und dynamischen mechanischen Eigenschaften von Kohlenstoff-Nanoröhren und Kohlenstoff-Nano-Peapoden mit Defekten. Acta Phys. Sin., 2019, 68(16): 166101. doi: 10.7498/aps.68.20190594
[2] [1] Xu T, Shen W, Huang W, et al.Fullerene Micro/Nanostructures: Controlled Synthesis and Energy Applications[J].Materials Today Nano, 2020.DOI:10.1016/j.mtnano.2020.100081.
Weiterführende Lektüre:
Wesentliche elektronische Materialien: Teil 2 - Siliziumkarbid

 Bars
Bars
 Perlen & Kugeln
Perlen & Kugeln
 Bolzen & Muttern
Bolzen & Muttern
 Tiegel
Tiegel
 Scheiben
Scheiben
 Fasern & Stoffe
Fasern & Stoffe
 Filme
Filme
 Flocke
Flocke
 Schaumstoffe
Schaumstoffe
 Folie
Folie
 Granulat
Granulat
 Honigwaben
Honigwaben
 Tinte
Tinte
 Laminat
Laminat
 Klumpen
Klumpen
 Maschen
Maschen
 Metallisierte Folie
Metallisierte Folie
 Platte
Platte
 Pulver
Pulver
 Stab
Stab
 Blätter
Blätter
 Einkristalle
Einkristalle
 Sputtering Target
Sputtering Target
 Rohre
Rohre
 Waschmaschine
Waschmaschine
 Drähte
Drähte
 Umrechner & Rechner
Umrechner & Rechner
 Schreiben Sie für uns
Schreiben Sie für uns
 Chin Trento
Chin Trento


