Alles, was Sie über MoO3-Nanopartikel wissen sollten
Einführung
Molybdäntrioxid ist eines der Übergangsmetalloxide mit der chemischen Formel MoO3(H2O)n (n=0 bis 3). MoO3 wird in einer Vielzahl von Anwendungen eingesetzt, z. B. als Photokatalysator, in der Optik, in der Gassensorik, in Batterien, in elektronischen Geräten und so weiter. Wasserfreies MoO3 bildet eine verzerrte "MoO6"-Oktaederstruktur, deren orthorhombischer Kristall in Abbildung 1 dargestellt ist. Die grünen Kugeln sind Molybdän und die roten Kugeln sind Sauerstoff. MoO3 hat 3 verschiedene Kristallstrukturen: α-orthorhombische, β-monokline und h-hexagonale Phasen. Die verschiedenen MoO3-Strukturen verleihen ihnen unterschiedliche physikalische und chemische Eigenschaften. Das h-MoO3 weist eine Phasenstabilität bis zu 436℃ auf, aber das α-MoO3 zeigt einen irreversiblen Phasenübergang unter 436℃ [1].

Abbildung 1: Struktur von MoO6-Oktaedern
Herstellung von MoO3-Nanostrukturen und Diskussion über die Synthese durch Verbrennung
Es gibt mehrere synthetische Methoden zur Herstellung von Molybdäntrioxid-Nanopartikeln:
Hydrothermale Synthese: Molybdänsalze wie Ammoniummolybdat reagieren mit Wasserstoffperoxid in einer wässrigen Lösung bei hoher Temperatur und hohem Druck zu MoO3-Nanopartikeln.
Solvothermische Synthese: Molybdänsalze reagieren mit einem organischen Lösungsmittel wie Ethanol unter hoher Temperatur, um MoO3-Nanopartikel zu bilden.
Co-Präzipitation: Eine Molybdänsalzlösung reagiert mit einem Fällungsmittel, z. B. einem Metallhydroxid oder -carbonat, bei einem bestimmten pH-Wert, und MoO3-Nanopartikel werden aus der Lösung ausgefällt.
Synthese durch Verbrennung der Lösung: Molybdänsalze vermischen sich mit einem Brennstoff-Oxidationsmittel-Gemisch und verbrennen unter hoher Temperatur, um MoO3-Nanopartikel zu bilden.
Es gibt noch viele andere Synthesewege, die hier nicht erwähnt sind. Für weitere Informationen oder bei Interesse wenden Sie sich bitte an Stanford Advanced Materials. Selbst bei einer Synthese führen unterschiedliche Parameter zu verschiedenen Arten von MoO3-Nanostrukturen. Nehmen wir als Beispiel die Solution Combustion Synthese.
Lösen Sie Ammoniumheptamolybdat (NH4)6Mo7O24-4H2O in destilliertem Wasser und mischen Sie die Lösung mit einem organischen Lösungsmittel (hier verwenden wir Harnstoff, EDTA, PEG 200 und Sorbitol als verschiedene organische Zusätze für die Experimente). Erhitzen und rühren Sie die Lösung, bis sich die Ausfällungen bilden. Der letzte Schritt besteht darin, die Ausfällungen zu erhitzen, um organische Zusätze und andere Verunreinigungen zu entfernen [2].
Ammoniumheptamolybdat (AHM) ist ein großes, komplexes Molekül, das häufig als Vorläufer bei der Herstellung von Mo-Verbindungen verwendet wird. Die chemische Gleichung für die Verbrennungssynthese der AHM-Lösung lautet
MoO3 kann sich auch ohne Zusatzstoffe bilden, aber die Zusatzstoffe spielen eine wichtige Rolle für das Kristallwachstum und die MoO3-Kerne. Verwenden Sie ein Rasterelektronenmikroskop (REM), um die Mikrostrukturen zu erkennen, die durch die Verwendung verschiedener organischer Zusatzstoffe entstehen. Wir erhalten die folgenden Beobachtungen: Harnstoff erzeugt eine kugelförmigere Morphologie als die anderen 3 Zusatzstoffe. PEG 200 erzeugt größere submikroskopische und weniger kugelförmige Nanopartikel. Sorbitol und EDTA erzeugen ganz unterschiedliche Nanostäbchen [2]. Dies ist auf die chemische Struktur der organischen Zusatzstoffe zurückzuführen. Abbildung 2 zeigt die chemische Struktur dieser vier organischen Zusatzstoffe. Harnstoff hat Stickstoff mit einem nicht bindenden Elektronenpaar. PEG200 und Sorbitol haben Sauerstoff in der OH-Gruppe. EDTA hat beide Stickstoffe mit einem nicht bindenden Elektronenpaar und Sauerstoff in der OH-Gruppe. Bei der Ligandenbildung ist der Stickstoff mit 2 freien Elektronen größer als der Sauerstoff. Daher ist Harnstoff leichter in der Lage, Mo aus AHM anzuziehen und Kerne mit einer geringeren Größe zu bilden als PEG200 und Sorbitol [2].
EDTA hat 2 Stickstoff mit 2 freien Elektronen und 4 Sauerstoff in OH. Es könnte auf den ersten Blick das am besten geeignete Additiv für die Herstellung von MoO3-Nanopartikeln sein. Aber EDTA ist, wie bereits erwähnt, eine sehr große, komplexe Verbindung. Der sterische Hinderungseffekt verhindert, dass der Stickstoff von EDTA Mo anzieht. Nur die Sauerstoffgruppe ist an der Ligandenstruktur beteiligt und bildet die Mikrostrukturen von MoO3 [2].
PEG200 hat nur eine Sauerstoffgruppe auf beiden Seiten. Es ist nicht so attraktiv wie Harnstoff, was bedeutet, dass es eine geringe Möglichkeit hat, MoO3 gleichzeitig auf beiden Seiten zu bilden. PEG200 ist jedoch eine sehr einfach strukturierte Verbindung mit einem geringen sterischen Hinderungseffekt. Für PEG200 ist es einfacher, einen Liganden zu bilden als für EDTA [2].
Wenn eine der Sauerstoffgruppen von Sorbitol an Mo bindet, ist es für die andere Sauerstoffgruppe aufgrund der linearen Struktur unmöglich, an ein anderes Mo zu binden. Insgesamt ist Sorbitol kein guter Zusatzstoff für die Herstellung von MoO3-Nanopartikeln [2]. Andere Bedingungen wie der pH-Wert, die Reaktionstemperatur, die Mo-Konzentration und das Verhältnis von Mo und Zusatzstoff können ebenfalls die Eigenschaften der hergestellten MoO3-Nanopartikel beeinflussen.
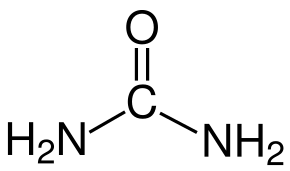
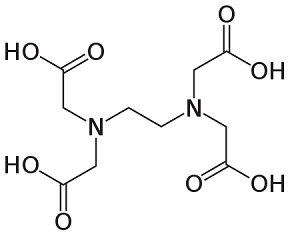
Harnstoff EDTA
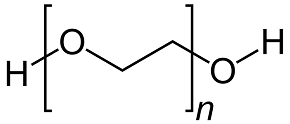
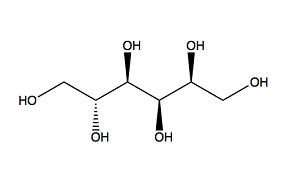
PEG200 Sorbitol
Abbildung 2: Molekulare Strukturen der im Experiment verwendeten organischen Zusatzstoffe
MoO3 Anwendungen
MoO3-Membranen haben gute elektrochrome Eigenschaften. Im Vergleich zu anderen Materialien wie WO3 und TiO2 hat MoO3 eine kürzere Reaktionszeit. Außerdem färbt sich MoO3 grau, wenn es einen elektrischen Reiz erkennt. Seine Absorptionskurve ist im sichtbaren Bereich gleichmäßig. Die Absorptionsspitze liegt in der Nähe von 550 nm, also in der Nähe der Empfindlichkeitsbande des menschlichen Auges. Die Herstellung von hochwertigem MoO3 mit Hilfe von MoO3-Nanopartikeln ist eine der beliebtesten Forschungsarbeiten.
PVC ist ein weit verbreitetes thermoplastisches Polymermaterial, das jedoch beim Verbrennen dichten Rauch erzeugt. Das Übergangsmetall zeigt eine gute Rauchunterdrückung. Durch die Kombination von 2 oder mehr Arten von Übergangsmetallverbindungen kann der dichte Rauch von PVC stark eingeschränkt werden. PVC birgt aufgrund des Zusatzes von Weichmachern erhebliche Brandgefahren in der Anwendung. MoO3 zeigt auch eine gute Flammhemmung. Kombiniert man MoO3 mit Cu2O, ergibt sich ein Synergieeffekt, der die Kosten für reine MoO3-Zusatzstoffe senken und die guten Eigenschaften der Kabel erhalten kann.
MoO3 ist ein hocheffizienter Photokatalysator. Im Gegensatz zur herkömmlichen Behandlung von Abwasserfarbstoffen können Nano-Photokatalysatoren Schadstoffe in harmlose Produkte wie CO2 umwandeln [3]. Durch die Nanopartikel erhält MoO3 eine größere Kontaktfläche, was eine schnellere Abbaugeschwindigkeit ermöglicht.
MoO3 ist ein n-Typ-Halbleiter, der in zahlreichen Anwendungen wie der Gasdetektion eingesetzt werden kann. Metalloxid-Gasdetektoren "wandeln" Gas in Elektrizität um, was schneller und einfacher ist als bei anderen Detektoren. Im Gegensatz zu anderen Metalloxid-Gasdetektoren ist MoO3 ein Halbleitermaterial mit breiter Bandlücke und aktiven Stellen auf seiner Oberfläche, die selektiv mit dem zu messenden Gas reagieren. MoO3 hat sehr gasempfindliche Eigenschaften. Es zeigt eine Empfindlichkeit gegenüber NH3, H2, CO und anderen Gasen bei etwa 450℃. Reine MoO3-Membranen funktionieren aufgrund ihrer hohen Temperaturempfindlichkeit und Selektivität nicht gut. Durch die Kombination mit anderen Materialien kann die Gasempfindlichkeit von MoO3 verbessert werden. Die Kombination von MoO3 mit V2O5 zur Herstellung von Membranen zeigt beispielsweise eine hohe Empfindlichkeit bei niedrigen Temperaturen (etwa 150℃) für NO2, NH3, CO, CH4, SO2 und H2.
Es gibt eine Vielzahl von Anwendungen für MoO3-Nanopartikel, die hier nicht erwähnt werden. Stanford Advanced Materials (SAM) bietet verschiedene Arten von MoO3 an. Wenn Sie weitere Informationen über MoO3 wünschen, können Sie sich mit Ihren Anwendungsinformationen an unser technisches Personal wenden und sich beraten lassen.
Referenz
- Pannipa Wongkrua, Titipun Thongtem, Somchai Thongtem, "Synthesis of h- and α-MoO3 by Refluxing and Calcination Combination: Phase and Morphology Transformation, Photocatalysis, and Photosensitization", Journal of Nanomaterials, Vol. 2013, Article ID 702679, 8 Seiten, 2013. https://doi.org/10.1155/2013/702679
- Parviz, D., Kaz→emeini, M., Rashidi, A. M., & Jafari Jozani, K. (2009). Synthese und Charakterisierung von MOO3-Nanostrukturen durch Lösungsverbrennung unter Verwendung von Morphologie- und Größenkontrolle. Journal of Nanoparticle Research, 12(4), 1509-1521. https://doi.org/10.1007/s11051-009-9727-6
- Thekkethil, A. J., Sreekuttan, S., & Madhavan, A. A. (2021). Anwendung von Nano-Molybdäntrioxid in der Wärmespeicherung und Photokatalyse. Journal of Physics: Conference Series, 2070(1), 012120. https://doi.org/10.1088/1742-6596/2070/1/012120

 Bars
Bars
 Perlen & Kugeln
Perlen & Kugeln
 Bolzen & Muttern
Bolzen & Muttern
 Tiegel
Tiegel
 Scheiben
Scheiben
 Fasern & Stoffe
Fasern & Stoffe
 Filme
Filme
 Flocke
Flocke
 Schaumstoffe
Schaumstoffe
 Folie
Folie
 Granulat
Granulat
 Honigwaben
Honigwaben
 Tinte
Tinte
 Laminat
Laminat
 Klumpen
Klumpen
 Maschen
Maschen
 Metallisierte Folie
Metallisierte Folie
 Platte
Platte
 Pulver
Pulver
 Stab
Stab
 Blätter
Blätter
 Einkristalle
Einkristalle
 Sputtering Target
Sputtering Target
 Rohre
Rohre
 Waschmaschine
Waschmaschine
 Drähte
Drähte
 Umrechner & Rechner
Umrechner & Rechner
 Chin Trento
Chin Trento



